Подготовка образцов в микроскопии
Существует множество причин для исследования клеток и тканей человека. Медицинские и биологические исследования опираются на знания о стандартном строении и функционировании клеток и тканей, и структур, которые они составляют. В здоровом состоянии клетки и другие тканевые элементы организованы на основе постоянных и узнаваемых форм. Изменения, вызываемые воздействием широкого спектра химических и физических факторов, выражаются в структурных изменениях на микроскопическом уровне. Для многих заболеваний характерны структурные и химические аномалии, отличающиеся от нормального состояния. Выявление этих изменений и привязка их к конкретным заболеваниям является основой патогистологии и цитопатологии, важными специальностями современной медицины. Микроскопия играет важную роль в гематологии (исследования крови), микробиологии (изучение микроорганизмов, в том числе паразитов и вирусов), и в более широком смысле в областях биологии, зоологии и ботаники. Во всех этих дисциплинах образцы изучаются с помощью микроскопа.
Микроскопия
Существует много различных видов микроскопии, но наиболее часто используемый – это светлопольная микроскопия, в которой образцы просвечиваются пучком света, проходящим через них (в отличие от пучка электронов в электронной микроскопии). Общие требования к образцам для наиболее эффективного исследования с помощью светлопольной микроскопии:
- Клетки и другие элементы в образце должны храниться в «жизнеподобном» состоянии (данный процесс называется «фиксация»);
- Образец должен быть прозрачным, нежели светонепроницаемым, для того, чтобы свет мог проходить через него;
- Образец должен быть тонким и плоским, то есть должен присутствовать только один слой клеток;
- Некоторые компоненты должны быть дифференциально окрашены, так они смогут быть четко различимы.
Способы подготовки
Из-за требований микроскопии подготовка образцов ограничена следующими способами:
- Целостное закрепление образца, при котором весь организм является достаточно небольшим и тонким для того, чтобы быть размещенным непосредственно на предметном стекле микроскопа;
- «Сплющивание» образца, при котором клетки специально сплющены на предметном стекле для того, чтобы раскрыть их содержание (например, растительные образцы, где клетки разрушаются для выявления хромосом);
- Мазки, где образец состоит из клеток, находящихся в жидкости (например, в крови, сперме или спинномозговой жидкости), или где отдельные клетки соскребаются с поверхности или аспирируются (всасываются) из органа (эксфолиативная цитология). Мазки являются основой известного теста Папаниколау, используемого для выявления рака шейки матки у женщин;
- Резка, при которой образцы удерживаются таким образом, чтобы была возможность отрезать от них тонкие фрагменты, закрепить на предметном стекле и окрасить. Фрагменты подготавливаются с использованием специального прибора – микротома
Из всех этих вариантов только целостное закрепление и резка позволяют сохранить структурные связи между отдельными клетками и внеклеточными компонентами. Мазки и сплющивание предоставляют детальные сведения об отдельных клетках и относительном числе клеток, однако структурные связи утрачиваются. Подготовка срезов является технически наиболее сложным из этих методов, так как требует специализированного оборудования и значительного опыта. Микроскопическое исследование срезов патологоанатомами является краеугольным камнем в диагностике рака. Хотя методика подготовки срезов из животного и растительного материала одинакова, последующее описание относится к тканям животных (человека).
Подготовка срезов
Самая свежая ткань является очень чувствительной к воздействиям, легко подверженной к деформациям и повреждениям, и поэтому невозможно подготовить тонкие фрагменты (срезы), если образец не поддерживается во время резки. Также обычно образец нуждается в «фиксации» перед подготовкой срезов. В целом существуют две стратегии, которые могут быть использованы для того, чтобы обеспечить эту поддержку.
- Ткани могут быть быстро заморожены и поддерживаться в таком состоянии во время резки с использованием криостатного микротома (микротом в морозильной камере). Такие фрагменты называются «замороженными срезами». Замороженные срезы могут быть подготовлены очень быстро, и поэтому используются, когда интраоперационное исследование необходимо для проведения хирургических процедур или тогда, когда необходимо избежать любого вмешательства в химический состав клеток (как при некоторых гистохимических исследованиях).
- В качестве альтернативы, образцы могут быть пропитаны жидким веществом, которое впоследствии может быть преобразовано в твердое тело, обладающее необходимыми физическими свойствами, что позволит отрезать от него тонкие фрагменты. Используются различные вещества для пропитки и поддержки образцов, в том числе эпоксидная смола и смолы метакрилата, но гистологический парафин является самым популярным средством для обычной световой микроскопии. С его помощью получают так называемые «парафиновые срезы». Такие срезы обычно подготавливаются с использованием роторного микротома. Слово «роторный» описывает способ резки данного инструмента. Во всех гистопатологических лабораториях парафиновые срезы подготавливают почти из всех образцов и используют в диагностике.
В нижеследующих пунктах описываются основные шаги при подготовке парафиновых срезов. Эти шаги в целом диктуют план и рабочий процесс в крупных, специализированных гистопатологических лабораториях, где ежедневно обрабатываются сотни образцов.

Рис. 1. Срез для диагностики подготавливается с помощью криостатного микротома. Срез, полученный из мгновенно замороженной ткани снимается на теплое стекло, где он будет незамедлительно зафиксирован и окрашен.

Рис. 2. Роторный микротом используется для подготовки парафиновых срезов. На переднем плане лента из срезов «выходит» готовой для крепления к стеклу микроскопа.
Получение образцов
Образцы, полученные для гистологического исследования, могут происходить из ряда различных источников. Они варьируются от очень крупных экземпляров или целых органов до крошечных фрагментов ткани. Например, ниже приводятся несколько типов образцов обычно получаемыми в гистопатологических лабораториях.
- Удаленные образцы (хирургическая биопсия), где целые органы или поврежденные участки удаляются при операции;
- Образцы, полученные с помощью инцизионной биопсии, где для диагностики ткань забирается с пораженного участка;
- Образцы, полученные с использованием щипковой биопсия, при которой используется круговое лезвие для того, чтобы удалить небольшой участок подозрительной ткани для исследования (часто из кожи);
- Скарификационная биопсия, где маленькие фрагменты ткани срезаются с поверхности (как правило, кожи);
- Кюретажная биопсия, при которой маленькие кусочки ткани удаляются со слизистой оболочки матки или шейки матки;
- Сердцевинная биопсия, когда небольшой образец удаляется с помощью специальной иглы, иногда через кожу (перкутанно).
Образцы обычно получают в фиксаторе (консерванте), но иногда они поступают свежими и должны быть незамедлительно зафиксированы. До того, как образцы будут приняты в лаборатории, маркировки и сопроводительные документы тщательно проверяются, все детали записываются, и начинается "отслеживание образца".
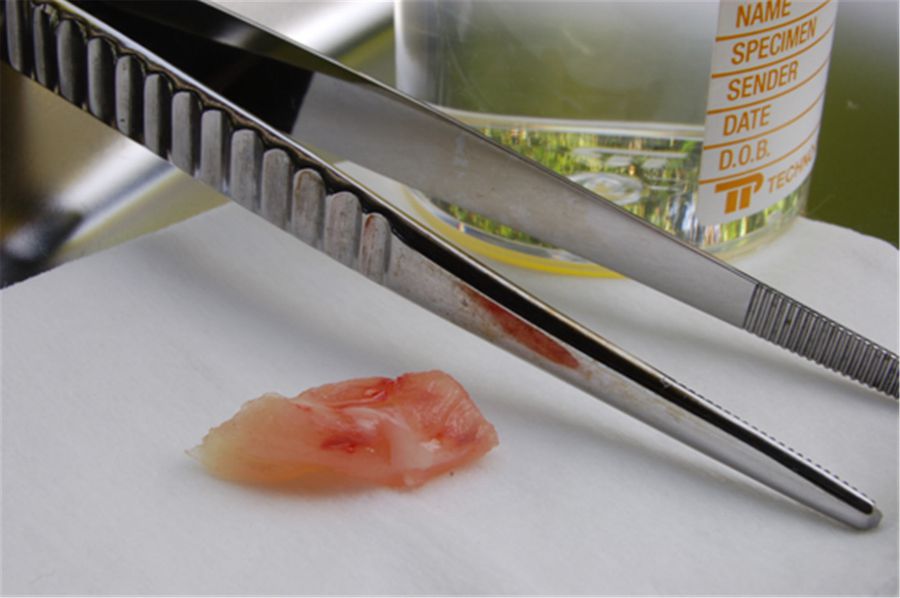
Рис. 3. Свежие, незафиксированные образцы после хирургического удаления. Чтобы предотвратить дегенерацию или высыхание образца, он должен быть зафиксирован как можно скорее.
Фиксация
Фиксация является важнейшим шагом в процессе подготовки образцов для микроскопического исследования. Ее цель заключается в предотвращении процесса разрушения и сохранении клеток и тканей в «жизнеподобном» состоянии. Это происходит путем остановки активности ферментов, уничтожения микроорганизмов и затвердевания образца при сохранении достаточной молекулярной структуры, позволяющей использовать необходимые методы окрашивания (в том числе с применением реакции антиген-антитело и других реакций, в зависимости от сохранения ДНК и РНК). Чем раньше начат процесс фиксации после отделения образца от кровоснабжения, тем лучше будет результат. Самый популярный фиксирующий агент – это формальдегид, обычно в форме натрий-фосфатного буфера (часто упоминается как «формалин»). В идеале образцы должны быть зафиксированы путем погружения в формалин на срок от шести до двенадцати часов, прежде чем они будут использоваться.

Рис. 4. Хирургические образцы в процессе фиксации в формалине. Обратите внимание, что объем консерванта значительно превышает размеры образцов. Кассета, в которой будут находиться образцы во время обработки, уже имеет маркер с идентификаторами пациента.
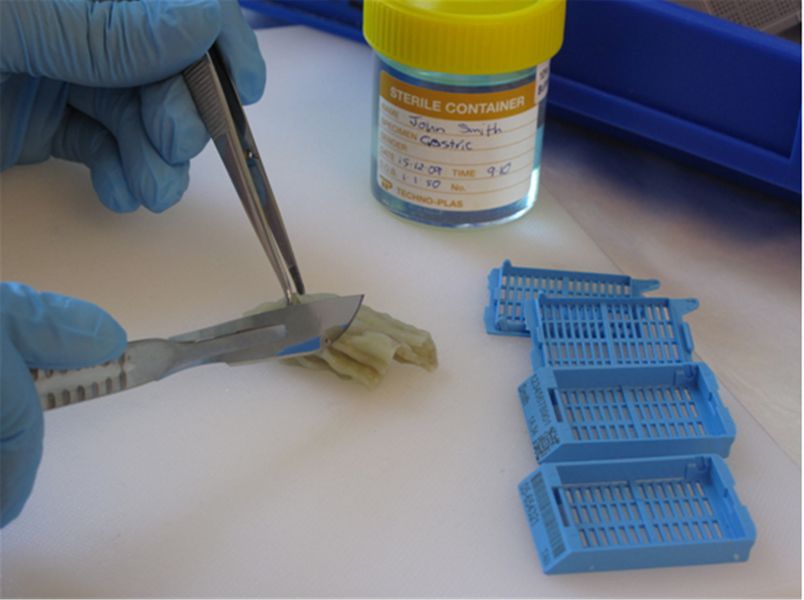
Рис. 5. Этот хирургический образец желудка был зафиксирован в формалине. Элементы толщиной около 4 мм теперь будут взяты из соответствующих областей и помещены в маркированные кассеты для обработки.
Обработка
Для больших партий образцов, подготовка «парафиновых срезов» автоматизирована с помощью инструмента под названием «тканевый процессор». Эти инструменты позволяют образцам последовательно пропитываться различными растворителями и расплавленным парафином, завершающим данный процесс. В начале образцы находятся в водной среде (на водной основе) и должны пройти через несколько преобразований: обезвоживание и очистка растворителями (как правило, этанолом и ксилолом), прежде чем быть помещенными в расплавленный воск (который является гидрофобным и не смешивается с водой). Длительность и детали промежуточных шагов «плана обработки» для конкретной партии будут зависеть от происхождения и размера образцов. План может быть, как один час для небольших образцов, так и двенадцать часов или более для больших образцов. Во многих лабораториях основная обработка проводится ночью. Из-за стремления улучшить рабочий процесс и сократить сроки, в настоящее время оказывается заметное давление на лаборатории с целью использовать процессоры, способные производить быструю обработку.


Рис. 6. Тканевый процессор загружается корзиной с кассетами, содержащими образцы ткани для обработки. Подробные сведения о процессе обработки и план отображаются на экране процессора.
Заливка
После обработки образцы помещаются в заливочный центр, где они извлекаются из кассет и помещаются в формы, заполненные парафином. На этом этапе образцы аккуратно ориентируются, потому что это будет определять плоскость, через которую они будут разрезаны на фрагменты, а также определять, будут ли аномальные зоны видны через микроскоп. Кассеты, в которых производилась обработка, содержат данные для идентификации образцов, и теперь они помещаются сверху формы и закрепляются добавлением парафина. Блоку образцов дают затвердеть на холодной поверхности, а затем форма снимается. Кассеты, заполненные парафином, являются неотъемлемой частью блока и обеспечивают устойчивую основу для зажима в микроскопе. Блок, содержащий образец, готов для резки на фрагменты.

Рис. 7. Заливочный центр помогает оператору, так как объединяет холодную панель, горячую панель и контролируемый поток расплавленного парафина.

Рис. 8. Образец желудка размещен и ориентирован в заливочной форме на горячей панели заливочного центра.

Рис. 9. Блок готов для микротомии. Образец желудка, который был обработан и залит, готов к подготовке срезов с помощью микротома. Бледно-синяя кассета была использована для того, чтобы держать образец во время обработки, и сейчас является частью «блока». Она будет зажата в держателе образца, и фрагменты будут отрезаны от лицевой части блока.
Резка
Фрагменты отрезаются с помощью высокоточного инструмента, называемого «микротом», который использует очень тонкие стальные лезвия. Парафиновые срезы обычно отрезают при толщине в 3-5 мкм, гарантируя, что срез состоит только из одного слоя клеток (красные клетки крови имеют диаметр около 7 мкм). Одним из преимуществ парафина, как заливочного агента, является то, что при резке фрагменты будут держаться вместе от края до края, образуя «ленты» из срезов. Это делает обработку проще.
Теперь срезы «выходят» на поверхность теплой воды в флотационной ванне для того, чтобы разгладить их, а затем снять на предметные стекла микроскопа. После тщательной просушки они готовы к окрашиванию.

Рис. 10. Лента со срезами отрезается от парафинового блока с помощью роторного микротома. Обратите внимание, что срезы толщиной 4 мкм (4/1000 миллиметра) показывают малую деформацию и разрушение.

Рис. 11. Парафиновый срез устанавливается на стекло микроскопа после теплой воды, использованной для разглаживания.
Окрашивание
Помимо нескольких естественных пигментов, таких как меланин, клетки и другие элементы, составляющие большинство образцов бесцветные. Для того, чтобы выявить структурные детали с помощью светлопольной микроскопии, используются некоторые способы окрашивания. Окраска гематоксилином и эозином (H&E) повсеместно используется как отправная точка для предоставления важнейшей структурной информации. С помощью этого метода ядра клетки окрашиваются синим, а цитоплазма и многие дополнительные клеточные компоненты окрашиваются в оттенки розового. В гистопатологии многие состояния могут быть выявлены путем исследования только H&E.Однако иногда требуется дополнительная информация для того, чтобы обеспечить полную дифференциальную диагностику, а это требует дальнейшего, более специализированного метода окрашивания. Это могут быть «специальные пятна», сделанные с помощью красителей или металлических вкраплений для определения конкретной структуры микроорганизмов, или это могут быть иммунно-гистохимические методы, охватывающие расположение диагностически полезных белков с помощью отмеченных антител. Молекулярные методы, такие как гибридизация in-situ (ISH), также могут быть необходимыми для выявления специфических последовательностей ДНК или РНК. Все эти методы могут быть применены на парафиновых срезах, и в большинстве случаев полученные срезы полностью стабильны и могут храниться в течение многих лет.
После окрашивания, срезы покрываются покровным стеклом, после чего отправляются к патологоанатому, который будет рассматривать их под микроскопом, чтобы поставить правильный диагноз и подготовить отчет.
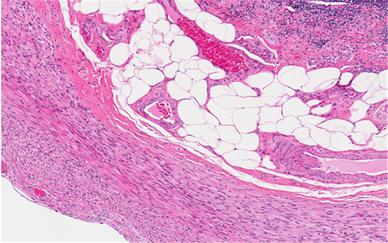
Рис. 12. Окраска гематоксилином и эозином. Это микроскопическое изображение (микрофотография) парафинового среза стенки человеческого аппендикса, полученное с помощью светлопольной микроскопии. Клетки окрашены синим цветом, а гладкие мышцы, коллаген и другие компоненты открашены в оттенки розового. Большие пустые пространства относятся к жировым клеткам, жиры были растворены во время обработки.

Рис. 13. Стойка для парафиновых срезов загружается в автоматизированный инструмент для окраски гематоксилином и эозином. Этот инструмент позволит окрасить элементы, а прилегающая система по подготовке срезов приложит покровное стекло, чтобы сохранить их и обеспечить оптимальные оптические условия для микроскопии.
Geoffrey Rolls
Geoffrey Rolls, консультант по гистологии, Leica Biosystems, Мельбурн, Австралия, имеет большой практический опыт и опыт в преподавании гистологии и гистотехнологии, в том числе 30 лет в качестве старшего преподавателя кафедры лабораторной медицины университета RMIT в Мельбурне, Австралия. Он имеет научную степень и профессиональное членство в австралийском Институте молодых ученых. Имеет большой интерес к гистотехнологии, особенно в областях обработки тканей, микротомии и общего образования по гистологии. В последние десять лет он выступал в качестве консультанта для Leica Biosystems.
Geoffrey.Rolls@leicabiosystems.com
Перевод статьи http://www.leicabiosystems.com/pathologyleaders/an-introduction-to-specimen-preparation






